Résumé de section
-

-
Nous sommes ravis de vous présenter notre nouveau cours en ligne sur les notions générales en thermodynamique. Ce cours interactif et accessible vous permettra de comprendre les bases de cette discipline fascinante, sans quitter le confort de votre domicile.
-
Bienvenue sur le chat du cours "Notion générale en Thermodynamique" !
Ici, vous pouvez poser toutes vos questions instantanément et obtenir des réponses en temps réel. Notre équipe d'enseignants et les autres étudiants sont là pour vous aider à approfondir votre compréhension de ce cours.
Nous sommes impatients de vous voir actif sur le chat et de partager des discussions enrichissantes avec vous.

-
Ce forum destiné aux étudiants de la première année, spécialité FPST
Bienvenue sur le forum dédié au chapitre " Notion générale en thermodynamique" !
C'est l'endroit idéal pour discuter, poser des questions et partager vos réflexions sur les concepts fascinants abordés dans ce chapitre. Nous encourageons les échanges d'idées entre les étudiants, car cela nous permet de bénéficier de différentes perspectives et de mieux appréhender les aspects complexes de la thermodynamique.
N'hésitez pas à partager vos expériences d'apprentissage, vos découvertes intéressantes ou même vos défis rencontrés lors de l'étude de ce premier principe.
 vous avez des questions, les membres de la communauté et
les enseignants seront là pour vous aider et vous fournir des réponses claires
et précises.
vous avez des questions, les membres de la communauté et
les enseignants seront là pour vous aider et vous fournir des réponses claires
et précises.
-
-
La carte conceptuelle du module de Chimie 02 réorganisée et reformulée de la manière suivante :
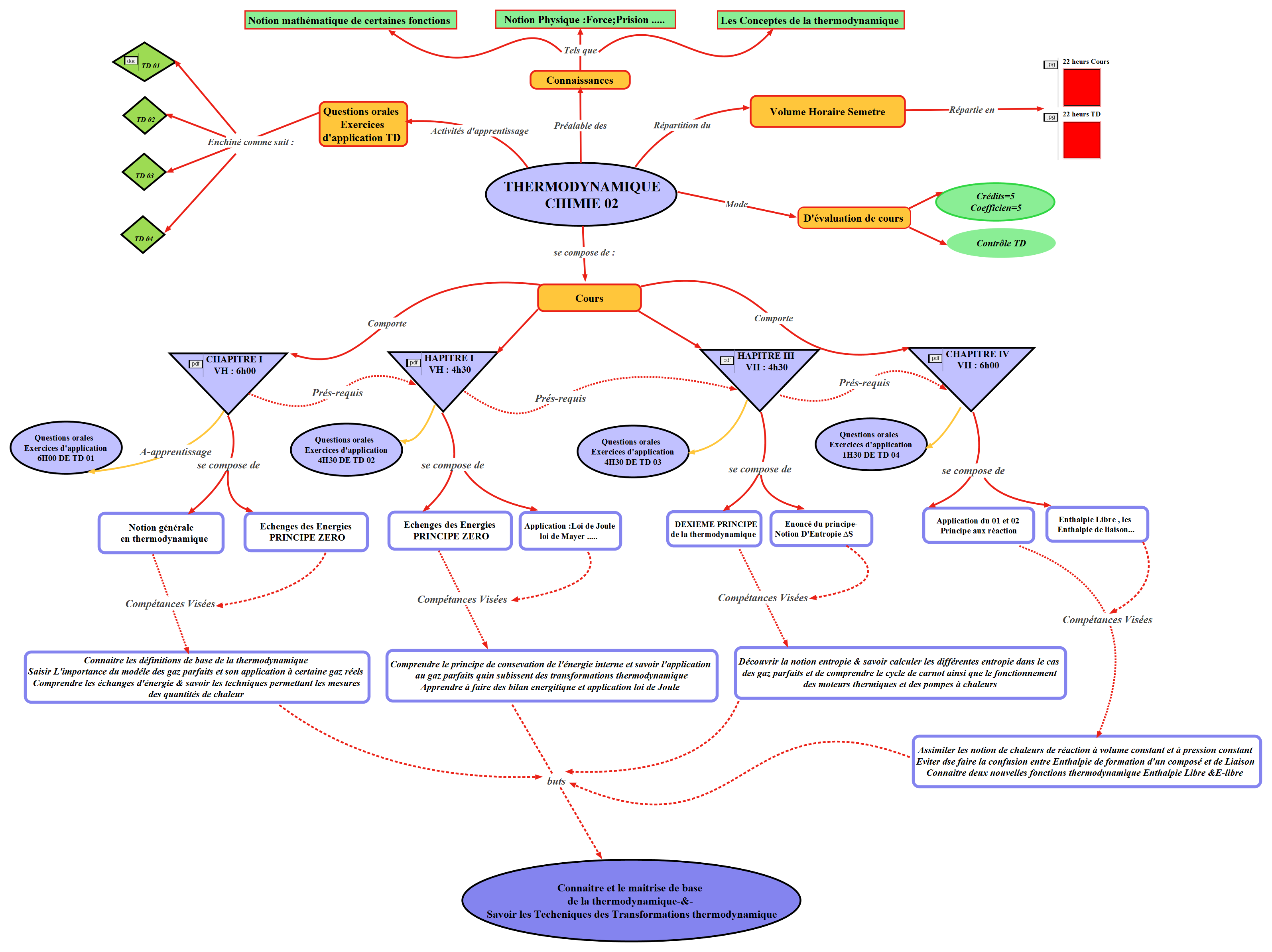
-
Faculté: Ecole Nationale Polytechnique d’Oran Maurice Audin
Enseignant : Cours, TD : Dr. Zouaoui .Rabha.Mourad
Contact : par mail au crmamourad@yahoo.fr / rabah-mourad.zouaoui@enp-oran.dz
Disponibilité : Au bureau : Mercredi, jeudi au Labo de Chimie de 11h00 -12h00
Département: Département de la Formation Préparatoire
Public cible : 1ère année UEF 1.2.2 - (Sciences Physiques)
Intitulé du cours : Chimie 02 (Thermodynamique)
Crédit: 05
Coefficient: 05

-
Ce cours a été conçu principalement pour les étudiants en sciences techniques (ST) et en sciences de la matière (SM), en particulier ceux qui sont inscrits en première année dans le département de formation préparatoire en science technologie. Il est également destiné aux étudiants de différentes spécialités qui suivent un enseignement général de chimie 02.
Ce cours est très pédagogique et se compose d'un texte clair et concis, ainsi que de nombreux schémas didactiques. Les bases théoriques sont présentées de manière logique et progressive au fil de chapitre, et des exercices corrigés sont inclus dans ce chapitre. Il est conforme aux programmes de la chimie 02 agréés par le ministère.

-
Plan de cours présenté par :
Dr Zououi Rabah Mourad
Maître de Conférences à l'ENP d'Oran – Maurice Audin
Département de Formation Préparatoire en Sciences & Technologies
-
-
Connaître les définitions de base de la thermodynamique
Saisir l’importance du modèle des gaz parfaits et son application à certains gaz réels
Faire la différence entre les types d’énergie

Comprendre les échanges d’énergie
Savoir les techniques permettant les mesures des quantités de chaleur lors des transformations thermodynamiques
Apprendre à faire des bilans énergétiques et application loi de Joule.

-
-
Température : Kelvin (K) · Celsius (°C) · Fahrenheit (°F).
-
Pression : Le "pascal" (symbole Pa).
-
Volume : m3, Litre.
-
Composition molaire x : sans unité.
-
Notions physiques : force, pression, travail, distance,……
-
Changements d’état physique (Liquide, vapeur, solide, gaz ….).
-
Notions mathématiques : différentielle totale exacte, fonction d’état.

-
-
Introduction
1. Définitions
1.1. Système & milieu extérieur
1.2. Les différents types de systèmes
1.3. État d'un système, variables d'état
1.4. Les variables d'état et fonctions d'état
1.5. Les variables qui ne sont pas fonctions d'état
1.6. Les transformations
1.7. Modèle de gaz parfait
1.8. Représentations graphiques des évolutions du système
1.9. Les gaz réels : gaz de Van der Waals
2. Échanges d'énergie
2.1. Chaleur et énergie
2.2. Principe zéro (équilibre thermique)
Références Bibliographiques
3. Test : QCM, Exercices
-
La thermodynamique est une science du macroscopique, manipulant de vastes ensembles de molécules, aux frontières parfois arbitraires et mouvantes, sous le nom commode mais abscons de « systèmes ». Elle requiert donc une analyse complète et circonstanciée des systèmes et des relations qu’ils entretiennent avec tout ce qui leur est extérieur. C’est la première difficulté à surmonter. Surtout, pour étudier les transformations de ces systèmes, mécaniques et thermiques, voire chimiques ou électromagnétiques, elle a recours à deux concepts qui, s’ils ont investi le vocabulaire courant, n’en restent pas moins très abstraits : « l’énergie » et « l’entropie ». On peut ressentir les effets de la pression ou de la température qui interviennent dans l’énergie et l’entropie, mais ces dernières, quant à elles, n’ont rien de sensible. Que la définition moderne de l’énergie et celle de l’entropie datent seulement du milieu du XIXe siècle suffit à montrer que ces grandeurs physiques sont le résultat d’un long travail de maturation chez les scientifiques. Aujourd’hui pourtant, dans la compréhension que les humains ont du monde et de son évolution, l’énergie et l’entropie jouent un rôle crucial. C’est qu’elles sont associées aux deux lois fondamentales de la nature, ou dans un autre sens de la définition de la thermodynamique qui est une discipline transversale de la physique, qui traite des transformations de l'énergie sous toutes ses formes. Elle est fondée sur deux principes fondamentaux : le premier principe énonce de façon très générale la conservation de l'énergie : l'énergie peut être stockée par un système sous forme d'énergie interne ou d'énergie cinétique, et peut être échangée avec l'extérieur sous la forme de travail ou de chaleur ; le second principe de la thermodynamique traite de l'évolution des systèmes, en introduit la notion essentielle d'entropie. La conjonction des deux principes permet de définir de façon très rigoureuse des conditions d'équilibre d'un système, c'est-à-dire l'état vers lequel il évoluera en fonction des conditions extérieures qui lui sont imposées.
-
Notion générale en thermodynamique présenté par :
Dr Zououi Rabah Mourad
Maître de Conférences à l'ENP d'Oran – Maurice Audin
Département de Formation Préparatoire en Sciences & Technologies
-
-
Le contenu du premier chapitre en premier lieu ,englobe les notions générales en thermodynamique résumé par une introduction à la thermodynamique structuré comme suit :- Définitions : systèmes ouvert, fermé, isolé, thermoélastique, variables d’état et fonctions d’état, grandeurs intensives et extensives, transformations réversibles et irréversibles, Comportement des gaz aux basses pressions : Diagramme de Clapeyron, variation des coordonnées d’Amagat en fonction de la pression, échelle absolue des températures, Modèle de gaz parfait: Equation d’état d’un gaz parfait, loi de Boyle-Mariotte, loi de Charles, loi de Gay-Lussac ; mélanges de gaz : nombre de moles, fraction molaire, pression partielle, Les gaz réels : Comparaison entre gaz parfait et gaz réel, équation de Van der Waals. En seconde lieu, ce chapitre englobe les échanges d’énergie définie par deux parties, en premier par chaleur et énergie ; - Notion de température, équilibre thermique : Principe zéro de la thermodynamique, différents types d’énergie, chaleur avec changement de température, transfert de chaleur, capacités thermiques, chaleur avec changement d’état, chaleur latente, mesures des quantités de chaleur, calorimétrie et la deuxième résume le travail mécanique effectué par une force de pression.
-
710.0 Ko
-
7.0 Mo
-
-
1- Thermodynamique chimique, M. Chabanel, éditions Ellipses.
2- Thermodynamique, R. Gaboriaud, éditions Ellipses.
3- Thermodynamique PCSI MPSI PTSI, 1ère année - Edition Aout 2007 ; Collection : Classe Prépa (Auteur) M. Pullicino.
4- Exercices corrigés de thermodynamique MPSI-PCSI-PTSI : Fiches, méthodes et exercices corrigés 1ère année, Xavier Ducros ; Date de parution : 29/06/05 ; Editeur : Ellipses Marketing ; Collection : Taupe-Niveau ; ISBN : 2-7298-2519-3
5- Thermodynamique. Cours et exercices corrigés, 1ère année MPSI-PCSI-PTSI (Broché) ; Jean-Robert Seigne
-
Evaluation
-
évaluation finale
-
Les exercices sont présentés à chaque fois avec leur correction détaillée, ils répondent au double souci d'expliciter les notions présentées dans le cours, et de préparer aux épreuves écrites.
-
-
Prenez le temps de répondre à chaque question de manière détaillée et précise.
-
Ce devoir porte sur les notions générales en thermodynamique et comporte trois parties : QCM, questions ouvertes et problèmes.
La première partie consiste en un QCM où vous devrez choisir la bonne réponse parmi plusieurs propositions concernant la définition de la thermodynamique, la première loi, la température.
La deuxième partie comprend des questions ouvertes où vous devrez expliquer la différence entre un système ouvert, fermé et isolé en thermodynamique, décrire le premier et le deuxième principe de la thermodynamique, donner un exemple concret d'application de la thermodynamique dans la vie quotidienne, et expliquer le concept de cycle thermodynamique avec un exemple.
Il est important de montrer vos calculs et d'expliquer vos réponses de manière claire et concise.
Bon travail
-